matterguy
ngs to all SOHA members! And what a busy Spring it has been! Our Apr
Southwest Oral History Association Newsletter Sum...
We Make Possible
The SEWO S1250 Motorised Tripod Turnstile Gate is ...
This project has been assisted by the Australian Government through th
1963 / 1965 /2014Jeténova MilneDigitised footage ...
Persimmon (Diospvros kaki L.) fruit are1996: Paull and Armstrong, 1994
tive treatment. 'Fuyu' persimmon fruit toler- or J...
Barracuda Networks
• CASE STUDY • Pioneering DIY retailer...
USEFUL JAPANESE PHRASES
Good morningWhat is this? Do you speak English ? O...
Our "Living Letters" delegation was warmly welcomed by the Haiti Prote
1 This sad reality is blindingly obvious simply by...
Mituna oyo bato batunaka mingi
FAQs - Lingala -- lokasa19 Soki nazali na likoki ...
POCO - User Manual
Document Version: 0.4 Draft, 5/01/19
av industrial products telephone 44 0 116 2461 261 fax 44 0
44 Flexpress AV Catalogue copy 5:Layout 1 31/08/2...
FOR PUBLICATIONUNITED STATES COURT OF APPEALSFOR THE NINTH CIRCUIT ...
E LIZABETH L ONA , AKA Lisa Elizabeth Lona, AKA ...
General Information
REGISTRATION All continuing students in good acade...
Mobility and Transfers
CONSIDERATIONS: 1. Canes redistribute weight from ...
Rev. Brasil. Biol., 61(2):SPATIAL AND TEMPORAL ORGANIZATION OF AQUATIC
a, 2 a, 4 a, 5 a e 6 a Rev. Brasil. Biol., 61(2):2...
CODA Summer 2020 Page 1
2019-2021 Commission on DentaO Accreditation �...
The Fair Penitent Nicholas Rowe
Lisa Reid and Laura Manuel. Nicholas Rowe. Born on...
“The First aim of any activity is to reach perfect love and a deeply intimate, familiar and unend
Hahu. . obras. … 1799 - 1808. Encontro. . impo...
Kankaankuvioinnin eri tapoja
Lastakangas. Aurinkotekniikka. Savupainanta. Ruost...
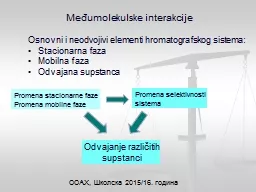
ООАХ, Школска 201
5. /1. 6. . година. Međumolekulske interakc...
Description : Think your cooking is the best? Then enter
our . competition and find out! We’ll be competi...